HeLa cell: ชีวิตอมตะของ Henrietta Lacks
ใน ปี 1951 หญิงสาววัย 30 ปีแห่งรัฐเวอร์จิเนีย สหรัฐอเมริกา เข้ารับการรักษาในโรงพยาบาลที่มีชื่อเสียงระดับโลกแห่งหนึ่ง-Johns Hopkins Hospital เธอได้รับการวินิจฉัยว่าเป็นโรคมะเร็งปากมดลูก อาการของโรคดังกล่าวลุกลามอย่างรวดเร็วและรุนแรง เธอเสียชีวิตในเวลา 8 เดือนต่อมา
ไม่ใช่ทุกส่วนในร่างกายของ Henrietta Lacks ที่สิ้นชีวา เซลล์มะเร็งของเธอยังคงมีชีวิตอยู่ ดำเนินกิจกรรมภายในเซลล์อย่างปกติ เจริญเติบโตและแบ่งตัวอย่างไม่มีที่สิ้นสุด--จวบจนเวลาปัจจุบัน
รูปถ่าย Henrietta Lacks ครั้งยังมีชีวิตครบทั้งร่าง
หาก แต่เซลล์มะเร็งที่ว่านั้นไม่ได้เจริญบนร่างกายที่ ไร้ชีวิตของ Henrietta Lacks เนื่องจากในระหว่างการผ่าตัดเพื่อพิสูจน์ชิ้นเนื้อมะเร็ง (cervical biopsy) มีชิ้นส่วนเนื้อเยื่อมะเร็งหลงเหลือ ชิ้นส่วนดังกล่าวซึ่งยังมีสภาพค่อนข้างสมบูรณ์และยังมีความสามารถในการเจริญ เติบโตได้ถูกส่งต่อไปยังนายแพทย์ George Gey ผู้เป็นหัวหน้านักวิจัยในโรงพยาบาล Johns Hopkins ในขณะนั้น ซึ่งมีขอบเขตความสนใจเกี่ยวกับระบบต่อมไร้ท่อ มะเร็ง และไวรัสวิทยา
เซลล์ มะเร็งของ Henrietta Lacks ได้ ปลุกความทะเยอทะยานของ Dr.Gey ที่คาดหวังถึงการพัฒนาอย่างก้าวกระโดดของวิทยาการเพาะเลี้ยงเนื้อเยื่อ (tissue culture หรือ cell culture) เนื่องจากเซลล์มะเร็งเป็นเซลล์ที่สามารถเจริญพัฒนาได้อย่างไม่สิ้นสุดหากมี การควบคุมสภาวะแวดล้อมอย่างเหมาะสมและมีอาหารหล่อเลี้ยงเพียงพอ การดำรงอยู่ของเซลล์มะเร็งของ Henrietta Lacks จะนำไปสู่การศึกษาและค้นพบกระบวนการทางชีววิทยาของเซลล์มะเร็ง-ซึ่งอาจนำไป สู่หนทางในการพิชิตเซลล์มะเร็งในอนาคตข้างหน้า Dr.Gey ประกาศเป้าหมายอันสูงส่งดังกล่าวต่อหน้าสาธารณชน (โดยนำ”เซลล์มะเร็ง”ของ Henrietta Lacks ใส่หลอดทดลองออกอากาศทางโทรทัศน์ด้วย) และเดินหน้าเพาะเลี้ยง ศึกษาเซลล์มะเร็งของ Henrietta Lacks อย่างต่อเนื่อง (‘the isolation and maintenance of normal and malignant or otherwise diseased tissues as temporary or stable organoids or as derived cell strains.’)
Dr. George Gey คนขวาด้านบน
เพื่อ เพิ่มความเข้าใจให้กับผู้ที่ไม่ได้เรียน ชีววิทยาระดับมหาวิทยาลัย จึงจำเป็นต้องอธิบายเกี่ยวกับการเพาะเลี้ยงเนื้อเยื่อ หรือ การเพาะเลี้ยงเซลล์ (tissue culture หรือ cell culture) อย่างคร่าวๆ การเพาะเลี้ยงเนื้อเยื่อคือการแยกเซลล์ชนิดเดี่ยวจากสิ่งมีชีวิตหนึ่งมา เลี้ยงโดยควบคุมสภาวะแวดล้อมให้เหมาะสมและให้สารอาหารหล่อเลี้ยงเซลล์ วัตถุประสงค์เพื่อทำการศึกษาระดับเซลล์ในงานวิจัยด้านวิทยาศาสตร์ในแขนง ต่างๆทั้งวิทยาศาสตร์บริสุทธิ์ (การศึกษาวงจรเซลล์, การศึกษาด้านอณูชีววิทยาหรือพันธุกรรม, การศึกษากระบวนการทางชีวเคมี ฯลฯ) และวิทยาศาสตร์ประยุกต์ (การทดสอบฤทธิ์ทางชีวภาพของสารเคมี, การศึกษากลไกการเกิดโรค, การผลิตโปรตีน ฯลฯ) ปัจจุบัน การเพาะเลี้ยงเซลล์ถือเป็นเครื่องมือพื้นฐานและมีการใช้อย่างกว้างขวางในการ ศึกษาทางชีวภาพ
เซลล์เพาะเลี้ยงสามารถแบ่งตามต้นกำเนิดได้เป็นสองชนิดหลักคือ Primary cell line และ Continuous cell line
Primary cell line คือเซลล์ที่แยกจากสิ่งมีชีวิตหรืออวัยวะของสิ่งมีชีวิตโดยตรง เช่น เซลล์ตัวอ่อนไก่ (Chicken embryo cell) เซลล์ไตสุนัข (Dog kidney cell) ข้อดีของ cell line ชนิดนี้คือ มีคุณสมบัติเหมือนเซลล์ที่อยู่ในสิ่งมีชีวิตทุกประการ สามารถใช้เป็นแบบในการศึกษาสรีรวิทยาปกติในอวัยวะนั้นๆได้ แต่ข้อเสียก็คือเลี้ยงได้ไม่นานนัก เซลล์จะมีกระบวนการแก่ชราและตายไปในที่สุด (สาเหตุคืออะไรจะอธิบายต่อไป)
Continuous cell line คือเซลล์ที่มีคุณสมบัติแบ่งตัวได้ไม่สิ้นสุด จึงสามารถเลี้ยงต่อไปได้เรื่อยๆไม่มีวันตายเช่น เซลล์มะเร็ง เซลล์ที่ติดเชื้อไวรัสบางชนิด จากคุณสมบัติดังกล่าวจึงอาจกล่าวได้ว่าเซลล์เหล่านั้นเป็นอมตะ ซึ่งจะเพิ่มสะดวกอย่างมากในการศึกษาวิจัย เนื่องจากสามารถเลี้ยงเซลล์ต่อไปได้เป็นร้อยๆรุ่น และไม่ต้องมีกระบวนการยุ่งยากในการแยกเซลล์ออกจากสิ่งมีชีวิตหรืออวัยวะ แต่ข้อเสียก็คือเซลล์ดังกล่าวมักมีการกลายพันธุ์ไปจากเซลล์ปกติ ดังนั้น การวิจัยจาก continuous cell line จึงมีขอบเขตจำกัดอยู่บ้าง โดยมากมักใช้ศึกษากระบวนการพื้นฐานทั่วไปของเซลล์ซึ่งไม่มีความแตกต่างกัน ระหว่างเซลล์ปกติกับ immortal cell
แน่นอนว่า เซลล์มะเร็งของ Henrietta Lacks จัดเป็น continuous cell line และเป็นเซลล์อมตะแรกๆของโลกเสียด้วย
เซลล์ มะเร็งของ Henrietta Lacks นั้นถูกตั้งชื่อใหม่ว่า HeLa (Henrietta Lacks) ตัว Dr.Gey นั้นมีความปรารถนาชื่อเสียงจากงานวิจัยดังกล่าวหรือไม่ก็ยากจะคาดเดา แต่การกระทำของเขาก็สร้างคุณประโยชน์นานัปการด้านวิทยาการเพาะเลี้ยงจวบจน ปัจจุบัน Dr.Gey ได้แจกจ่ายเซลล์มะเร็งดังกล่าวให้กับนักวิจัยอีกเป็นจำนวนมาก HeLa จึงแพร่กระจายไปทั่วโลกในเวลาไม่ช้า ถูกส่งต่อจากห้องปฏิบัติการหนึ่งไปยังอีกห้องปฏิบัติการหนึ่ง จากนักวิจัยคนหนึ่งไปยังนักวิจัยอีกหลายคน จนมีคำกล่าวว่ายุคดังกล่าวเป็น ‘ยุคของ HeLa’ (HeLa era)
และการใช้ประโยชน์จาก HeLa cell ก็ส่งผลให้เกิดการพัฒนาทางการแพทย์อย่างก้าวกระโดดดังที่ Dr.Gey คาดคะเน มีงานวิจัยจำนวนมากที่ศึกษาชีววิทยาระดับเซลล์โดยใช้ HeLa cell และทำให้เกิดการค้นพบ ความเข้าใจสิ่งใหม่ๆ เป็นต้นว่า กลไกการเกิดเซลล์มะเร็ง กลไกการติดเชื้อ HIV ผลของรังสีและสารพิษต่อเซลล์ การทำแผนที่ยีน (gene mapping) และความสำเร็จที่ไม่พูดถึงไม่ได้คือ การผลิตวัคซีนโปลิโอแบบฉีดใน HeLa cell โดย Dr.Jonas Salk (ดังนั้นวัคซีนดังกล่าวจึงถูกเรียกว่า Salk polio vaccine)
แต่ กระนั้น Henrietta Lacks ก็ไม่ได้รับการอ้างถึงใดๆในฐานะที่เป็นเจ้าของเซลล์แม้แต่น้อย (ในเวลาดังกล่าว HeLa cell ถูกเข้าใจผิดว่ามาจากชื่อเต็ม HeLen Lane หรือ Harriet Lane ด้วยซ้ำ) อันที่จริงแล้ว เซลล์มะเร็งของเธอถูกนำไปใช้โดยปราศจากความยินยอมของเธอ (inform consent) และแม้แต่ญาติพี่น้องของเธอก็ไม่ได้รับรู้การกระทำดังกล่าวด้วยซ้ำจนกระทั่ง เวลาผ่านไปหลายต่อหลายปีหลังจากที่ Dr.Gey เสียชีวิตไปนานแล้ว และความพยายามที่จะปกปิดชื่อแท้จริงของ HeLa นั้นต้องเป็นอันสิ้นสุด
บาง คนอาจเกิดคำถามในใจว่าการกระทำดังกล่าวเป็นเรื่องผิดจริยธรรมหรือไม่ ประเด็นดังกล่าวถูกนำมาพิจารณาครั้งหนึ่งในศาลแห่งรัฐแคลิฟอร์เนียและได้รับ การตัดสินว่า “ชิ้นส่วนเนื้อเยื่อของบุคคลใดๆที่ถูกทิ้ง ไม่ถือเป็นสมบัติของผู้นั้นอีกต่อไป และสามารถถูกนำมาใช้ในเชิงการค้าได้” ดังที่กล่าวมา ต้นกำเนิดของ HeLa นั้นเป็นเพียงชิ้นส่วนเนื้อเยื่อที่หลงเหลือจากการผ่าตัด แน่นอนว่าจากคำตัดสินดังกล่าวคงสร้างความกังขาแม้กระทั่งผู้อ่านที่กำลัง อ่านบล็อกนี้ ประเด็นหนึ่งที่น่าคิดคือโรงพยาบาล John Hopkins เป็นโรงพยาบาลที่มีชื่อเสียงระดับโลก และ HeLa cell ก็ถูกนำไปใช้ประโยชน์อย่างมากมายมหาศาล…หากลองพิจารณาตามทฤษฎีประโยชน์นิยม ก็…อืม…นะ (อย่างไรก็ตาม ดูเหมือนว่าลูกหลานของ Henrietta Lacks ไม่พอใจกับเหตุการณ์ที่เกิดขึ้นเท่าไรนัก และพวกเขาก็ค่อนข้างเจ็บปวดกับการปิดบังความลับนานนับสามสิบปีดังกล่าว)
รูปโรงพยาบาล John Hopkins วิทยาลัยทางการแพทย์ชื่อดังระดับโลก
เซลล์ มะเร็งคือเซลล์ที่เกิดการกลายพันธุ์ของยีน เป็นผลให้สูญเสียการควบคุมกรแบ่งตัวเพิ่มจำนวนตนเอง เซลล์มะเร็งสามารถถูกกระตุ้นให้เกิดได้จากปัจจัยหลายประการเช่น การบาดเจ็บของเซลล์ รังสี สารเคมี เชื้อจุลินทรีย์บางชนิด
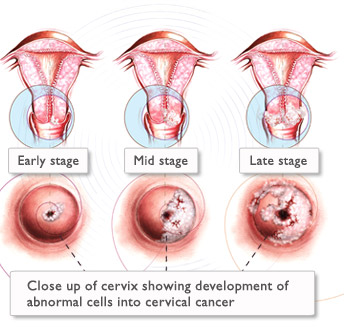
HeLa cell มีชิ้นส่วนจีโนมของไวรัส Human papilloma virus (HPV) อยู่ในสารพันธุกรรม ซึ่งแน่นอนว่า Henrietta Lacks ติดเชื้อไวรัสดังกล่าวขณะที่เธอยังมีชีวิตอยู่และเป็นสาเหตุที่ทำให้เธอเป็น มะเร็ง HPV นั้นได้รับการพิสูจน์มาเป็นเวลาช้านานแล้วว่าเป็นสาเหตุสำคัญอย่างหนึ่งที่ กระตุ้นให้เกิดมะเร็งปากมดลูกในมนุษย์ (จนกระทั่งบริษัทยาแห่งหนึ่งกล้าเคลมว่า หากมนุษย์ทุกคนได้รับการฉีด HPV vaccine แล้วไซร้ มะเร็งปากมดลูกจะถูกกำจัดจากโลกนี้โดยสิ้นเชิง บริษัทไหนไม่รู้ลองไปค้นหาดูเองนะจ๊ะ) ด้วยคุณสมบัติความเป็นมะเร็งของ HeLa cell นั้นเองทำให้มันเป็นอมตะและสามารถแบ่งตัวได้อย่างไม่สิ้นสุด
HPV เป็นสาเหตุในการเกิดมะเร็งปากมดลูก
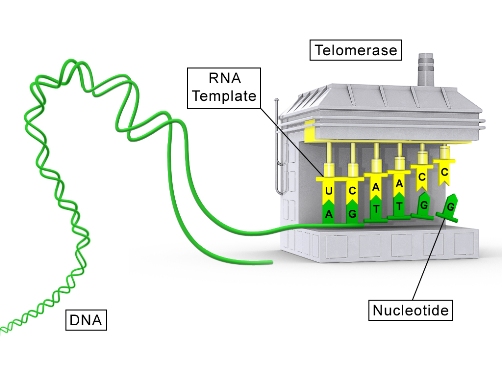
ใน เซลล์ปกติจะมีกระบวนการแก่ชราของเซลล์ (cell senescence) ซึ่งทำให้เซลล์สามารถแบ่งตัวได้อย่างจำกัดจำนวนครั้ง กระบวนการหนึ่งที่มีบทบาทสำคัญคือการหดสั้นของเทโลเมียร์ (telomere shortening) หากยังไม่ลืมชีววิทยาม.ต้นกันไปหมด เทโลเมียร์คือหน่วยพันธุกรรมส่วนปลายของโครโมโซม และเนื่องจากข้อจำกัดบางประการของกระบวนการเพิ่มจำนวนสารพันธุกรรม (DNA replication) จะทำให้เทโลเมียร์มีการหดสั้นลงทุกครั้งในแต่ละรอบของการแบ่งเซลล์ (หากอธิบายต่อจะซับซ้อนมาก ถ้าสนใจลองค้นคว้าดูเองโดยใช้ key word “end replication problem” ซึ่งเกี่ยวกับ Okasaki’s fracment) การหดสั้นลงของเทโลเมียร์ทำให้สารพันธุกรรมทั้งหมดของเซลล์ไม่สมบูรณ์ และทำให้เซลล์ตายในที่สุด
ในเซลล์มะเร็งหลายชนิดรวมถึง HeLa cell จะมีเอ็นไซม์ telomerase ซึ่งไม่พบในเซลล์มนุษย์ปกติ (ยกเว้นเซลล์สืบพันธุ์ เซลล์ต้นกำเนิด (stem cell) ในบางระยะ) ทำหน้าที่ต่อสายเทโลเมียร์ที่หดสั้นลงแต่ละรอบของการแบ่งเซลล์ ทำให้เทโลเมียร์มีความยาวคงที่ และกระบวนการแก่ชราของเซลล์ทุกยับยั้ง นี่เป็นสาเหตุที่ HeLa cell สามารถแบ่งตัวได้อย่างไม่มีที่สิ้นสุด
และ เนื่องจาก HeLa cell ถูกส่งต่อและมีการใช้อย่างแพร่หลายทั่วโลกจวบจนปัจจุบัน อาจกล่าวว่า HeLa cell มีอายุมากกว่าเจ้าของร่างของมันเสียแล้ว จำนวนเซลล์ทั้งหมดก็คงมากกว่าเซลล์ที่ประกอบเป็นร่างกายของ Henrietta Lacks ไม่รู้กี่ร้อยที่พันเท่าเช่นกัน (เป็นเรื่องยากมากที่จะคำนวณว่า HeLa cell มีการแบ่งตัวมาแล้วกี่ครั้งนับจากวันแรกที่ถูกแยกออกจากเจ้าของร่าง นอกจากต้องนับห้องปฏิบัติการที่มีอยู่ทั่วโลกแล้วยังต้องรวมถึงการส่งต่อ HeLa cell อย่างไม่เป็นทางการ-ให้เปล่าจากมือหนึ่งไปยังอีกมือหนึ่ง-ด้วยไมตรีต่อกัน ของนักวิจัยในห้องปฏิบัติการเดียวกันอีกด้วย) ซ้ำร้าย HeLa cell ได้ก่อปัญหาสำคัญที่สุดอย่างหนึ่งในการเพาะเลี้ยงเนื้อเยื่อ คือ การปนเปื้อนระหว่างเนื้อเยื่อ (tissue culture contamination)
การปน เปื้อนระหว่างเนื้อเยื่อ คือ การปนเปื้อนของเนื้อเยื่อชนิดหนึ่งในเนื้อเยื่อชนิดหนึ่ง โดยอาจเป็นสปีชี่ส์เดียวกันหรือไม่ก็ได้ ซึ่งเป็นเหตุการณ์ที่ไม่พึงประสงค์และเป็นปัญหาที่สำคัญมากในการศึกษาวิจัย ที่มีการเพาะเลี้ยงเนื้อเยื่อ อันเกิดขึ้นได้ในห้องปฏิบัติการที่ไม่มีการควบคุมอย่างมีประสิทธิภาพหรือ เกิดจากเทคนิคอันสะเพร่าของผู้วิจัย หรือแม้จะระวังสักเพียงใดก็ตามการปนเปื้อนก็ยังอาจเกิดขึ้นได้อยู่ดี! การปนเปื้อนของเนื้อเยื่อจะทำให้ผลการศึกษาที่ได้นั้นไม่ถูกต้องและไม่น่า เชื่อถือ (ต้องการผลการทดลองในเซลล์ชนิดหนึ่ง แต่กลับกลายเป็นผลการทดลองในเซลล์อีกชนิดหนึ่ง) ในยุคที่ HeLa cell มีการใช้อย่างแพร่หลาย cell line อื่นๆจำนวนมากในยุคดังกล่าวจึงถูกปนเปื้อนไปด้วย HeLa…เช่นเดียวกัน การปนเปื้อนดังกล่าวเกิดขึ้นทุกหนทุกแห่ง…ทั่วโลกนี้
ในปี 1967 Stanley Gartler ได้พัฒนาวิธีตรวจสอบการปนเปื้อน HeLa cell ใน cell line อื่นๆ เขาทำการตรวจสอบโปรตีน 2 ชนิดคือ glucose-6-phosphate dehydrogenase (G6PD) และ phosphoglucomutase (PGM) ซึ่งมีความแปรผันทางพันธุกรรมอันมีลักษณะจำเพาะในสตรีชาวแอฟริกัน-อเมริกัน Henrietta Lacks เป็นลูกครึ่งแอฟริกัน-อเมริกัน ดังนั้นฟีโนไทป์ของโปรตีนทั้งสองชนิดในเซลล์ของเธอจึงมีความจำเพาะ และสามารถใช้เป็น marker ตรวจวัดการปนเปื้อนใน cell line อื่นๆได้
การ ปนเปื้อน HeLa ส่งผลกระทบต่อวงการวิทยาศาสตร์หลากหลายแขนงที่มีการใช้เซลล์เป็นเครื่องมือ ศึกษา ตัวอย่างหนึ่งคือการศึกษาด้านรังสีวิทยา เมื่อนักรังสีวิทยาทำการทดสอบความสัมพันธ์ของขนาดของรังสีกับการตายของเซลล์ มนุษย์ โดยใช้เซลล์ไตมนุษย์ในการศึกษา เขามีอันต้องประหลาดใจเมื่อเซลล์เพาะเลี้ยงดังกล่าวปนเปื้อน HeLa ผลการทดลองที่ได้จำเป็นต้องถูกโยนทิ้ง เพราะแทนที่จะได้ผลของรังสีต่อเซลล์มนุษย์ปกติ กลับได้ผลของรังสีต่อเซลล์มะเร็ง
อย่างไรก็ตาม ปัญหาการปนเปื้อน HeLa ในปัจจุบันเป็นที่น่าวิตกกังวลน้อยลง เนื่องจากความก้าวหน้าทางวิธีการตรวจสอบซึ่งไม่ได้จำกัดอยู่แค่การตรวจฟีโน ไทป์ เทคนิคอื่นๆอย่าง karyotyping และ chromosome band analysis ก็ถูกพัฒนาขึ้นเพื่อตรวจสอบเช่นกัน ร่วมกับการควบคุมการปนเปื้อนในห้องปฏิบัติการอย่างมีประสิทธิภาพมากขึ้น ปัจจุบันพบว่า 42 ใน 252 human cell lines (18%) มีการปนเปื้อน HeLa
คุณสมบัติ และความเป็นอมตะของ HeLa cell ทำให้มีนักวิทยาศาสตร์จำนวนหนึ่งพิจารณาว่ามันไม่ใช่ ‘เซลล์มนุษย์’ อีกต่อไป นักวิทยาศาสตร์นามว่า Leigh Van Valen พยายามกำหนดให้มันเป็นสิ่งมีชีวิตสปีชี่ส์ใหม่ (Helacyton gartleri) ด้วยเหตุผลดังนี้- โครโมโซมของ HeLa cell มีความแตกต่างจากโครโมโซมมนุษย์ปกติ (HeLa มีโครโมโซม 82 แท่ง และมีชิ้นส่วนของจีโนมไวรัส HPV18 แทรกอยู่ด้วย)
- HeLa cell มีความสามารถในการเจริญเติบโต ซึ่งเหนือยิ่งกว่าการควบคุมของมนุษย์ที่ทำการเพาะเลี้ยง
อย่าง ไรก็ตาม การระบุสปีชี่ส์ใหม่ของ HeLa cell นั้นไม่ได้รับการยอมรับในแวดลงนักวิทยาศาสตร์สากล แม้ว่าจะมีการใช้อย่างแพร่หลายในกลุ่มคนจำนวนหนึ่งก็ตาม
ลอง พิจารณาอีกมุมองหนึ่ง โดยย้อนรอยกลับไปที่ชื่อของกระทู้นี้ เราสามารถกล่าวได้หรือไม่ว่า HeLa ก็ยังคงเป็น Henrietta Lacks และ Henrietta Lacks ยังคงมีชีวิตเป็นอมตะตราบเท่าที่ HeLa cell ยังแบ่งตัวต่อเนื่องอย่างไม่สิ้นสุด เพราะว่า HeLa cell นั้นครั้งหนึ่งก็เป็นเซลล์ในร่างกายของเธอ…เป็นส่วนหนึ่งในชีวิตของเธอมิใช่ หรือ คำถามนี้อาจเป็นคำถามปรัชญาที่ต้องขอยกคำพูดของนายแพทย์ Sir William Oslar ที่เคยปาฐกถาที่มหาวิทยาลัยฮาร์วาร์ดก่อนที่ Henrietta Lacks จะเกิดด้วยซ้ำว่า
‘‘the individual is nothing more than the transient off-shoot of a germ plasm, which has an unbroken continuity from generation to generation, from age to age . . . ‘the individual organism is transient, but its embryonic substance, which produces the mortal tissues, preserves itself imperishable, everlasting, and constant.’ ’’
ทั้งนี้ขออนุญาตไม่แปลเนื่องจากอาจทำให้เสียใจความสำคัญ หรืออีกนัยหนึ่งคือไม่มีความสามารถมากพอที่จะแปลประโยคซับซ้อนดังกล่าว…กร๊าก
ข้อ ถกเถียงเกี่ยวกับจริยธรรมในการใช้ประโยชน์จาก HeLa cell โดยไม่มีการขอความยินยอม หรือการตั้งสปีชี่ส์ใหม่ให้กับ HeLa cell หรือความเป็นอมตะของ Henrietta Lacks ก็ยังคงเป็นที่น่ากังขาต่อไป แต่อย่างไรก็ตาม HeLa cell ที่ Henrietta Lacks ได้หลงเหลือไว้ให้โลกนี้ก็ได้สร้างคุณประโยชน์ ความก้าวหน้าทางวิทยาศาสตร์อย่างมากมาย ดังนั้น จขกท.ขอแสดงความเคารพเธอจากใจจริงมา ณ ที่นี้ครับ
ปล. มีวันรำลึกแด่ Henrietta Lacks ด้วยนะ (Henrietta Lacks day) แต่กำลังสงสัยอยู่ว่าเป็นวันที่ 1 กุมภาพันธ์ (วันแรกที่ Henrietta Lacks เข้ารับการรักษา) หรือวันที่ 11 ตุลาคม (วันเกิดของ Henrietta Lacks) ของทุกปี -*-
หมาย เหตุ ชื่อบทความดัดแปลงมาจากหนังสือเรื่อง The Immortal Life of Henrietta Lacks เมืองไทยไม่มีขาย อยากได้ต้องสั่งซื้อทางอินเตอร์เน็ตนะจ๊ะ
Reference
Lucey PB, Nelson-Rees AW, Hutchins MG. Henrietta Lacks, HeLa Cells, and Cell Culture Contamination. Arch Pathol Lab Med. 2009; 133: 1463-1467.
O’Brien JS. Cell culture forensics. PNAS. 2001; 98(14): 7656-7658.
Holt ES, Wright EW, Shay WJ. Regulation of Telomerase Activity in Immortal Cell Lines. Molecular and Cellular Biology. 1996; 16(6): 2932-2939
Smith Van. Wonder Woman: The Life, Death, and Life After Death of Henrietta Lacks, Unwitting Heroine of Modern Medical. [Online], Accessed 13 December, 2009 at http://www.citypaper.com/news/story.asp?id=3426
http://en.wikipedia.org/HeLa



ไม่มีความคิดเห็น:
แสดงความคิดเห็น